Menü
Breadcrumbs
Inhalt
Biocatalysis Platform Zittau "BioPlatZ"
Allgemeine Informationen
| Projektnummer | 62457401 |
|---|---|
| Projekttitel laut Förderbescheid | Biocatalysis Platform Zittau |
| Akronym | BioPlatZ |
| Projektlaufzeit | 05.05.2017 - 31.08.2020 |
| Forschungsschwerpunkt | Energie und Umwelt |
| Projektkategorie | Forschung |
| Zuordnung | |
| Kompetenzfeld | Energie und Umwelt |
| Themengebiet | Chemokatalyse, Biokatalyse |
| Grundeinheit | Fakultät Natur- und Umweltwissenschaften |
Inhaltliche Projektbeschreibung
Biocatalysis Platform Zittau
Motivation
Ziel des vorliegenden Projekts ist es, neuartige energie- und ressourcenschonende Syntheseverfahren für Verbindungen zu entwickeln, die z. B. in Form von medizinischen Wirkstoffen eine hohe Anforderung an die Reinheit stellen. Unter Verwendung von ganzen Zellen bzw. isolierten Enzymen als Biokatalysatoren, soll eine selektive Transformation von Ausgangssubstanzen ermöglicht werden, die als Grundbausteine zur Synthese komplexer chiraler Moleküle dienen. Enzyme, die in mikrobiellen Zellen produziert und mit Hilfe gentechnischer Methoden optimiert werden können, besitzen ein nahezu unerschöpfliches Potential für innovative Entwicklungen. Sie sind in der Lage, vielfältige Stoffumwandlungen energieschonender, gezielter und umweltverträglicher durchzuführen, als das in vielen klassischen chemischen Prozessen möglich ist.
Kombiniert man moderne biokatalytische mit chemokatalytischen Ansätzen (Abbildung 1), ergibt sich eine völlig neue Qualität im Umwelt- und Ressourcenschutz und für die Nachhaltigkeit wirtschaftlicher Prozesse.
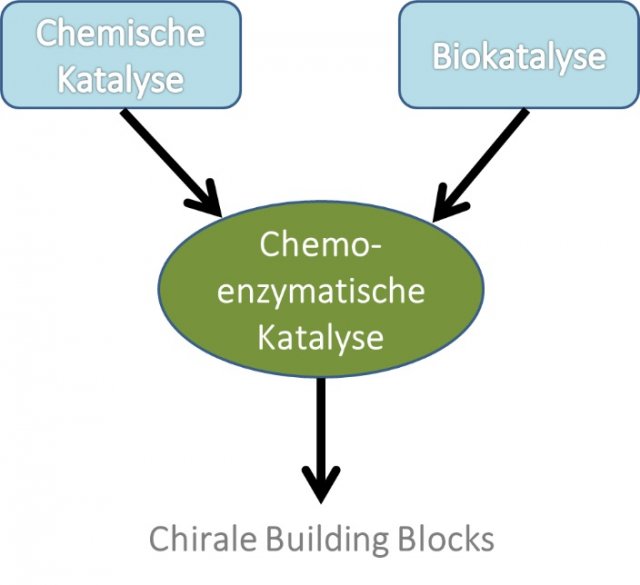
Abbildung 1: Chemoenzymatische Katalyse
Diese Kombination biotechnologischer und chemischer Ansätze ermöglicht die Einbeziehung biobasierter Rohstoffe bei einer nachhaltigen, energie- und umweltschonenderen Herstellung von Feinchemikalien als ‚high added-value‘ Produkt.
Das Projekt fokussiert die biotechnologische Herstellung chiraler β-Hydroxycarbonsäure-Derivate mit dem Ziel der Synthese chiraler Auxiliare bzw. building blocks, die anschließend für stereoselektive Synthesen von Feinchemikalien (Pharmazeutika und Pflanzenschutzmittel) eingesetzt werden können (Abbildung 2).
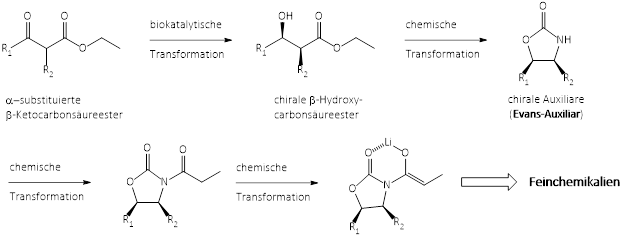
Abbildung 2: Chemoenzymatische Synthese chiraler Auxiliare bzw. building blocks für die anschließende stereoselektive Synthese von Feinchemikalien
Forschungsteam
Die Umsetzung dieser Ideen wird durch die Nachwuchsforschergruppe BioPlatZ verwirklicht (Abbildung 3). Die Mitarbeiter von BioPlatZ arbeiten in drei Arbeitsgruppen, die jeweils die wissenschaftliche Expertise der Leiter der Arbeitsgruppen repräsentieren.
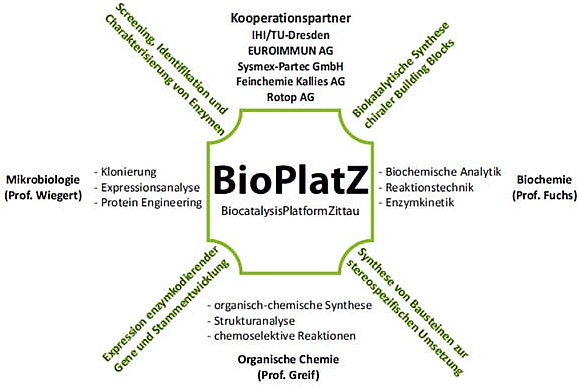
Abbildung 3: Nachwuchsforschergruppe (Biocatalysis Platform Zittau, BioPlatZ)
2 Teilprojekte unter der Kostenstellennummer 62417401:
Die Arbeitsgruppe Organische Synthesechemie und Strukturanalytik wird vom Prof. Dr. Dieter Greif geleitet und befasst sich mit der Etablierung neuer organisch-chemischer Synthesen, mit chemokatalytischer Methodenentwicklung sowie der gesamten Strukturanalytik der synthetisierten Verbindungen.
Unter Leitung von Prof. Dr. Annett Fuchs werden durch die Arbeitsgruppe Biochemie/Bioanalytik enzymbasierte Reaktionssysteme zur stereoselektiven Synthese von building blocks entwickelt. Untersucht und optimiert werden biochemische und chemische Analysenmethoden zur Umsetzung der Edukte, der Zusammensetzung der Produkte, der Raum-Zeit-Ausbeute sowie der erreichbaren Stereoselektivität.
1 Teilprojekt unter der Kostenstellennummer 62457401:
Herr Prof. Dr. Thomas Wiegert führt die Arbeitsgruppe Mikrobiologie/Molekularbiologie.
Im Fokus steht die Identifikation und Herstellung rekombinanter Enzyme für die stereoselektive Stoffumwandlung. Weiterhin sollen geeignete prokaryontische und eukaryontische Expressionssysteme etabliert werden sowie mikrobielle Stämme zur Ganzzellbiokatalyse entwickelt werden.

Abbildung 4: Nachwuchsforschergruppe BioPlatZ (von links: Prof. Dr. Thomas Wiegert, Prof. Dr. Annett Fuchs, Prof. Dr. Dieter Greif, Dr. Marek Pecyna, M.Sc. Corinna Schuster, M.Sc. Christian Trapp, M.Sc. Akadil Belgara, M.Sc. Chris Drewniok, Dr. Kateřina Barková; M.Sc. Philipp Röbisch nicht abgebildet).
Die bisher erzielten Ergebnisse
- 1) Entwicklung organisch-chemischer Synthesen kommerziell nicht erhältlicher
- alpha-substituierter ß-Ketocarbonsäureester
- 2) Etablierung und Optimierung der Methoden zur syn-selektiven Reduktion
- substituierter ß-Ketocarbonsäureester (Nachweis der Diastereoselektivität mittels
- NMR-Spektroskopie)
- 3) Entwicklung der HPLC-Methoden an einer chiralen Phase zur Bestimmung der
- Enantioselektivität der durchgeführten Reaktionen
- 4) Trennung racemischer Gemische mittels Candida antartica Lipase B (CAL B)
- 5) Selektive biochemische Reduktion von 2-Phenylacetessigester unter bevorzugter
- Bildung des Stereoisomers (2R, 3S)-3-Hydroxy-2-phenylbuttersäureethylester
- 6) Identifizierung potentieller Enzyme mit ß-Ketoreduktaseaktivität mit Hilfe von DNA-
- und Metagenomdatenbanken
- 7) Funktionale Expression mikrobieller Ketoreduktasen aus verschiedenen Hefen in
- Escherichia coli
- 8) Erfolgreiche Umsetzung unterschiedlich substituierter ß-Ketocarbonsäureester
- mit den gewonnenen rekombinanten Enzymen
- 9) Entwicklung entsprechender Methoden zur Umsetzung von
- ß-Ketocarbonsäureestern mittels Ganzzellsystemen für das Upscaling der
- Reaktionen im Multi-Bioprozessreaktorsystem
Projektverweise
Weitere Daten
-
Ansprechpartner
- Herr Prof. Thomas Wiegert (Projektleitung)
- Herr Chris Drewniok
- Herr Marek Pecyna
-
Fördermittelgeber
- 100310513 - ESF/SAB Nachwuchsforschergruppe 2017 - 2020

Finanzierung
- 27.725,51 €
Bilder
Bilder zum Vergrößern anklicken.
Schlagworte
Zurück zur Übersicht06.06.2026 18:12:15

